标题:Molecular mechanisms of Lycii Fructus (Goji berries) against xanthine dehydrogenase in hyperuricemia management: Integrating computational, metabolomic, and experimental approaches
原文链接:https://doi.org/10.1016/j.foodres.2025.115926
期刊:Food Research International
摘要
枸杞子(Lycii Fructus,LF),通常被称为枸杞,已显示出治疗高尿酸血症的潜力,但其潜在机制仍知之甚少。本研究结合基于网络的系统药理学、计算机辅助药物发现、非靶向代谢组学和实验方法,探讨枸杞的降尿酸作用。通过对3760种枸杞化合物-靶点相互作用的分子对接模拟,发现黄嘌呤脱氢酶(XDH)是关键靶点。在这些化合物中,黄豆苷元在分子动力学模拟中表现出最高的结合亲和力。代谢组学证实枸杞颗粒中存在黄豆苷元,且它能显著降低高尿酸血症斑马鱼模型的尿酸水平。进一步的体外实验和细胞热位移实验证实了其对黄嘌呤氧化酶的抑制作用。这些发现表明,黄豆苷元可能作为一种新型黄嘌呤氧化酶抑制剂,在保健品、功能性食品以及高尿酸血症药物开发中具有潜在应用价值。
引言
尿酸是人体嘌呤代谢的终产物(Li等人,2024)。黄嘌呤氧化还原酶是该途径中的关键酶,可催化次黄嘌呤氧化为黄嘌呤,进而氧化为尿酸(Siu等人,2006)。黄嘌呤氧化还原酶以两种胞质形式存在:黄嘌呤氧化酶(XOD)和黄嘌呤脱氢酶(XDH)(Rullo等人,2023)。由于生成增加或排泄减少导致的血清尿酸水平异常升高会引发高尿酸血症,其临床阈值设定为420μmol/L(7mg/dL)。男性为360μmol/L(6mg/dL),女性为360μmol/L(6mg/dL)(Johnson等人,2018年)。高尿酸血症与多种健康风险相关,包括尿酸钠晶体的形成,后者可通过激活含核苷酸结合域、富亮氨酸重复序列和 pyrin 域的3(NLRP3)炎症小体引发痛风(Wen等人,2024年)。高尿酸血症还与肾脏疾病、心血管疾病、肝脏疾病以及代谢综合征有关,代谢综合征包括肥胖、高血糖、高血压、高血脂和高胰岛素血症(Wen等人,2024年)。
目前,包括别嘌醇在内的降尿酸药物以及非布司他(Schlesinger等人,2023年)通过抑制黄嘌呤氧化还原酶来减少尿酸生成。然而,这些药物可能会产生严重的副作用,例如别嘌醇可能引发过敏反应,这就需要进行HLA-B*5801基因型检测,而非布司他则存在心血管和肝脏方面的风险(Stamp等人,2016年;Terkeltaub,2023年)。因此,目前迫切需要有效且安全的尿酸管理策略。
具有降尿酸作用的天然食品因其在高尿酸血症日常预防方面的潜力而备受青睐(Jenkins等人,2022年)。枸杞(Lycii Fructus,LF),通常被称为枸杞子,属于茄科枸杞属(Potterat,2010年)。它以其药用价值和营养价值而广受认可,在中国西北地区广泛种植,特别是在宁夏、甘肃、青海和内蒙古(Li等人,2019年)。由于其甜酸的味道,枸杞传统上用于中国家庭烹饪,在西方国家也有多种加工形式,如饼干、巧克力、什锦麦片、香肠、茶、果汁、葡萄酒和啤酒(Neelam等人,2021年)。现代药理学研究证实了枸杞的治疗功效,包括滋补肝肾、改善视力模糊、缓解腹痛以及减轻疲劳和头晕(Xiao等人,2022年)。
LF的化学成分包括多糖、类黄酮、花青素、原花青素、生物碱、酚酸和类胡萝卜素(Zhang等人,2024)。研究表明,LF提取物对小鼠的慢性高尿酸血症有作用(Sun等人,2017),并且对合并高尿酸血症的非酒精性脂肪肝患者有治疗益处(Zhang等人,2009)。尽管有这些发现,但LF降尿酸作用的分子机制以及负责这些作用的主要活性成分仍知之甚少。
为了更好地理解LF的降尿酸作用,我们采用了多方面的研究方法,结合了生物信息学、计算机模拟方法和实验验证。通过网络药理学、分子对接和分子动力学模拟,预测了LF作用中涉及的潜在活性化合物、关键分子靶点和信号通路。这些计算机模拟方法能够在分子水平上识别生物活性化合物及其相互作用。具体而言,网络药理学使我们能够分析LF成分与人类蛋白质之间的复杂相互作用,而分子对接和分子动力学模拟则有助于预测化合物与靶点的结合亲和力和稳定性。此外,我们还采用了非靶向代谢组学来识别LF中存在的活性化合物,从而深入了解其全身作用。随后,通过酶活性测定、细胞热位移分析和斑马鱼模型对这些计算分析的结果进行了实验验证,以确认所鉴定化合物的生理相关性和治疗潜力。这种综合方法旨在全面理解LF在高尿酸血症治疗中的作用机制,并发现管理该疾病的新治疗策略。
材料与方法
我们的研究过程概述如图S1所示。下文将简要介绍这些方法,详细描述请参见补充材料。
2.1. 计算机模拟分析
2.1.1. 基于网络的系统药理学分析
通过中药系统药理学数据库与分析平台(TCMSP)(Li等人,2022;Ru等人,2014;中国药典委员会,2020)识别出了LF的成分。通过其拼音“Gou qi zi”搜索LF,以获取分子标识符、PubChem CIDs、结构文件和药代动力学数据,并由多名团队成员进行了验证。SDF格式的结构文件以及SMILES序列通过PubChem检索获得。
潜在高尿酸血症靶点的确定分为三个步骤:从TCMSP数据库中检索LF化合物靶点,并使用SwissTargetPrediction(Daina等人,2019年)进行验证,重点关注具有\(probability >0.1\)预测值的靶点,以最大限度减少假阳性。从Open Targets平台(Ochoa等人,2023年、2021年)、GeneCards(Stelzer等人,2016年)和CTD(Davis等人,2023年)收集额外靶点,并通过UniProt(UniProt联盟等人,2023年)对基因名称进行标准化处理。
使用STRING数据库对蛋白质-蛋白质相互作用(PPIs)(Feng等人,2017;Szklarczyk等人,2021)进行了分析,重点研究“智人”,置信度得分为0.4(Chen等人,2023)。通过DAVID进行的GO富集分析(Sherman等人,2022;Zeng等人,2021)阐明了LF在降尿酸方面的功能作用,涉及的GO术语带有\(p<0.05\),而KEGG通路分析(Kanehisa,2000;Kanehisa和Sato,2020)则聚焦于人类特异性通路。
2.1.2. 结构下载与处理
从TCMSP数据库中筛选出的化合物被确定为潜在的对接配体,其3D结构来自PubChem或TCMSP的MOL2文件,并通过Discovery Studio Visualizer转换为PDB格式。蛋白质结构从NCBI BLAST或RCSB PDB数据库中获取,或使用AlphaFold预测(Jumper等人,2021年)。对于不完整的序列,通过SWISS-MODEL进行同源建模(Daina等人,2019年)。使用PyRx将蛋白质和配体结构转换为PDBQT格式以进行对接评估(Dallakyan和Olson,2015年)。
2.1.3. 枸杞化合物抗高尿酸血症靶点的高精度分子对接分析
分子对接在药物研发中至关重要(Kitchen等人,2004年),本研究使用AutoDock Vina(v1.1.2)进行分子对接,以评估LF化合物与高尿酸血症靶点之间的相互作用。对接模拟在神威·太湖之光超级计算机上运行,配体和蛋白质文件通过PyRx转换为PDBQT格式。对接盒确保了配体-蛋白质相互作用的全面分析,结合能低于-6.0千卡/摩尔表明具有强亲和力(Li等人,2023年)。
使用Autodock 4.2(Morris等人,1998年)进一步进行了针对黄豆苷元和黄嘌呤脱氢酶(XDH)的盲对接实验,其中包含了钼辅因子(钼蝶呤),并对Mo(VI)金属采用了AD4参数(Figueiredo,2017年)。对接参数和步骤的更多详细信息见补充材料与方法。
XDH受体采用1N5X结构。所有非极性氢与其成键碳合并,定义了可旋转键和扭转树,并使用MGL Tools 1.5.6(Sanner,1999)添加了Gasteiger电荷。生成的配体和受体的pdbqt文件作为输入文件。然后,使用AutoGrid 4.2围绕XDH受体的几何中心计算网格,网格间距为\(0.60 元\),盒子尺寸为\(75.6 ×75.6 ×75.6 \AA^{3},\),覆盖整个大分子作为盲对接的搜索空间。使用AutoDock 4.2进行对接计算,采用300次独立运行,运用拉马克遗传算法,所有其他参数均为默认设置。使用Discovery Studio Visualizer 2019分析预测的结合位置簇的分子间相互作用。
2.1.4. 化合物-靶点网络可视化
为了可视化配体-受体相互作用,我们使用了每个靶点结合能最高的前10种化合物来构建化合物-靶点网络(Li等人,2021)。使用Cytoscape(v3.9.1)构建该网络,其中度值表示每种化合物结合的靶点数量,节点的颜色和大小反映度值。
2.1.5. 化合物的结构聚类分析和分类
为了探究化合物结构与其之间的关系为了研究这些化合物针对高尿酸血症靶点的生物活性,我们使用OSIRIS DataWarrior(v5.5.0)和ClassyFire评估了所有化合物的理化性质。在DataWarrior中,我们对188种LF化合物的SMILES(表S2)及其与XDH的对接能进行了分析,以基于结构相似性和结合亲和力进行聚类(Sander等人,2015年)。ClassyFire(Djoumbou Feunang等人,2016年)为成员超过7个的聚类提供了化学分类。随后,我们将这些化合物与已知抑制剂进行了比较。
2.1.6. 药代动力学和毒性筛选
药物研发常常因药代动力学不佳和毒性问题而失败(Morgan等人,2012年),因此早期的ADMET评估至关重要。研究人员使用ADMETlab 2.0(https://admetmesh.scbdd.com/)对LF化合物进行了筛选。通过PAINS检测(Baell和Holloway,2010年)和Lipinski测试(Lipinski等人,2001年)评估了这些化合物的成药潜力。口服吸收情况通过人体肠道吸收来确定,而毒性则通过Ames试验(Mortelmans和Zeiger,2000年)和肝毒性结果进行预测。
2.1.7. 分子动力学模拟
使用分子动力学(MD)模拟结合SiBioLead平台(Wu等人,2024年)筛选潜在的高尿酸血症LF化合物,该平台用于蛋白质-配体预处理、能量最小化、平衡和生产运行。从分子对接结果中选取配体-蛋白质复合物,使用OPLS力场和GROMACS进行模拟。关键分析包括均方根偏差(RMSD)、均方根波动(RMSF)、\(R_{g}\)溶剂可及表面积(SASA)和氢键(H键)相互作用。补充材料(信息S1)中提供了更多细节和200纳秒的扩展模拟结果。
2.1.8. 关键活性结合位点的预测
我们使用了ProteinsPlus平台(Volkamer等人,2010年)及其DoGSiteScorer功能,基于3D结构预测潜在的蛋白质结合位点,即“口袋”。该平台计算了包括大小、形状和疏水性在内的口袋属性,并给出了药物可及性评分(0-1)(Volkamer等人,2012年)。上传PDB格式的蛋白质和SDF格式的配体后,共识别出49个潜在口袋,其中最大的P_0被选作进一步分析(数据S1和图S4)。
2.1.9. 配体-残基相互作用的3D结构可视化
根据对接结果,选择了具有最高平均结合亲和力的常见药物靶点XDH(PDB代码:2CKJ)进行配体结合位点分析。使用Discovery Studio Visualizer 2019可视化配体-残基相互作用,并通过ProteinsPlus平台识别关键的活性结合位点。对于结合在活性位点口袋内的化合物,评估了其与必需残基形成的氢键总数。
2.2. 枸杞的非靶向代谢组学分析
LF颗粒(批号A1119081)由广东一方制药有限公司生产,南方医科大学采用非靶向代谢组学结合质谱法对其进行了分析。使用赛默飞世尔科技™ Orbitrap Fusion™质谱仪和沃特世色谱仪进行提取和定量。在正离子和负离子模式下进行电喷雾电离后,进行超高效液相色谱分离和QE Plus质谱仪分析。使用Xcalibur 2.2处理数据,通过Compound Discoverer 3.3以及ChemSpider、MassList、mzCloud和mzVault等数据库进行化合物鉴定。实验条件的完整细节详见补充材料与方法。
2.3. 体内和体外实验
2.3.1. 材料与化学品
黄嘌呤氧化酶(XOD)购自上海麦克林生化科技有限公司,黄嘌呤钠盐(XSS)购自上海阿拉丁实业有限公司,氧嗪酸钾(PO)购自上海彼得医药科技有限公司。别嘌醇(APL)和羧甲基纤维素(CMC)购自美国Sigma-Aldrich公司,而黄豆黄素\((purity > 98 \% )\)购自美国MedChemExpress公司。磷酸盐缓冲液(PBS)购自武汉普赛生物科技有限公司。氧嗪酸钾分散于羧甲基纤维素中,黄嘌呤钠盐分散于鱼缸水中,黄豆黄素分散于二甲基亚砜中。黄嘌呤脱氢酶多克隆抗体购自Proteintech公司,β-肌动蛋白抗体购自Affinity Biosciences公司。Amplex® Red尿酸/尿酸酶检测试剂盒购自上海英潍捷基贸易有限公司。所有其他试剂均为市售分析纯。所有化学品的具体批号和目录详情见补充方法。
2.3.2. 斑马鱼实验
AB品系斑马鱼(Danio rerio)由南方医科大学斑马鱼模型与药物筛选研究所(中国广州)提供。所有实验均遵循机构动物护理和使用委员会的指南,并遵守《动物研究:体内实验报告指南》(Percie Du Sert等人,2020)(补充信息S1)。斑马鱼饲养在28℃的水中,水中含有200 mg/L海盐,电导率为450-550 S/cm,pH值6.5-8.5,硬度为50-100 mg/L \(CaCO_{3}\),光照周期为14小时光照/10小时黑暗。胚胎通过自然配对交配获得。幼鱼被随机分配到处理组和对照组以减少偏差,实验人员对分组情况不知情。处理方式是随机的,报告中注明了所有未控制的混杂因素。
180只受精后5天的幼虫被分为6组,每组30只,并用浓度梯度为0至100μM的大豆黄素进行处理。在72小时内评估死亡率,以确定最大耐受浓度(MTC)。最大耐受浓度被定义为无可见不良反应的最高浓度。高(最大耐受浓度)、中(1/2最大耐受浓度)和低(1/4最大耐受浓度)三种浓度被用于进一步测试。
2.3.3. 高尿酸血症模型的构建及尿酸水平测定
参照先前的一项研究(Zhang等人,2019年),使用200μM的PO和10μM的XSS建立了斑马鱼高尿酸血症模型,并以APL作为阳性对照。将六组各30条斑马鱼幼鱼(受精后5天的幼鱼)分别分配到对照组、高尿酸血症模型组,以及用低浓度(25μM)、中浓度(50μM)、高浓度(100μM)的黄豆苷元和100μM的APL处理的高尿酸血症组。
使用Amplex® Red尿酸/尿酸酶检测试剂盒(MolecularProbes®,美国)测定斑马鱼匀浆中的尿酸水平。共同处理后,将幼鱼在冰浴PBS中匀浆、离心,取25μL上清液转移至微孔板中,同时加入25μL反应缓冲液和50μL Amplex® Red试剂。将微孔板在37℃下孵育30分钟,然后测定560nm处的吸光度。尿酸浓度通过标准曲线计算得出。
2.3.4. 体外黄嘌呤氧化酶活性测定
由于XOD和XDH均由XDH基因编码,且共享相同的活性位点(Enroth等人,2000年;Harrison,2002年),我们进行了XOD酶活性测定,以验证关键分子对蛋白质活性的抑制率。采用Liu等人(2022年)的改良方法,使用酶标仪(SYNERGY,Biotek,7.5)在290nm处测定浓度为0.1、1、10和100μM的黄豆苷元的抑制活性,并加入黄嘌呤溶液,在美国37℃下孵育。每孔中加入50μL黄豆苷元、XOD溶液(0.1U/mL)、PBS(pH值),在℃下孵育10分钟,随后加入XSS并立即测量吸光度。对照组包括空白对照、完全反应对照和样品对照,别嘌醇作为阳性对照。抑制率采用以下标准公式计算: \[Inhibition ratio (\%)=\left(1-\frac{C_{3}-C_{4}}{C_{2}-C_{1}}\right) × 100 \%\] 其中,\(C_{1}\)为空白组,\(C_{2}\)为完全反应组,\(C_{3}\)为样品反应组,\(C_{4}\)为样品对照组。所有实验均进行三次重复,每个\(IC _{50}\)值以三次实验的平均值表示,\(IC _{50}\)值采用GraphPad Prism 9.0计算。
2.3.5. 细胞热位移分析
细胞热位移测定采用AML12细胞裂解物进行。将裂解物分成两份:一份用黄豆苷元处理(浓度为蛋白质浓度的十分之一),另一份用二甲基亚砜作为对照。在4℃下孵育2小时后,将裂解物在50–70℃下加热3分钟,冷却后离心。通过蛋白质印迹法分析可溶性组分。
蛋白质通过凝胶电泳分离,转移到膜上,封闭后与一抗在4℃下孵育过夜,随后与二抗孵育。使用化学发光法检测条带,并对条带强度进行定量分析,且以加载对照为基准进行标准化处理。
2.3.6. 统计分析
数据采用Prism 9.0进行分析,以均数±标准差表示。采用单因素方差分析和t检验,\(p-values <\) 0.05表示差异具有统计学意义。
结果
3.1. 枸杞化合物靶向的高尿酸血症蛋白预测
共选取了188种已知的LF化合物进行分子对接和靶点预测(表S1)。其中,通过TCMSP识别出301个靶点,而SwissTargetPrediction识别出648个独特靶点。通过Open Targets、GeneCards和CTD数据库预测高尿酸血症相关靶点。LF与高尿酸血症的重叠靶点被视为LF的高尿酸血症相关靶点(图1A)。最终确定了13个核心靶点:XDH、NOS3、MMP3、HTR2A、MAOA、PTGS2、ALDH2、ESR1、PPARG、APOB、IL6、TNF和VEGFA。
从DrugBank数据库中确定了7个作为高尿酸血症抑制剂的药物靶点,对应目前已获批的高尿酸血症治疗药物。这些靶点包括XDH(此前也被确定为核心靶点)、SLC22A8、SLC22A6、ABCC1、ABCC2、SLC22A11和SLC22A12。此外,目前处于高尿酸血症治疗2期临床试验的尿酸核苷转运蛋白抑制剂(BCX4208)以PNP为靶点,该靶点被新增为潜在药物靶点(Jenkins等人,2022年)。将LF-高尿酸血症交叉靶点与药物靶点相结合,用于后续研究(图1B)。
3.2. 分子对接证实了配体与靶点的结合
共对188种LF化合物与20个高尿酸血症相关靶点进行了对接,预测了结合亲和力、结合位点、取向和配体构象,得到3760个对接结果。对结合亲和力进行了评估,结合能越低(负值越大)表明亲和力越高(Jin和Wei,2024)。结合分数范围为-2.8至-12.1千卡/摩尔,平均亲和力为-6.6千卡/摩尔。
每个靶点的平均结合分数在-5.2至-7.5千卡/摩尔之间,总体平均值为-6.6千卡/摩尔。在排名前10的靶点中,GH01(XDH)的平均结合分数为-7.5千卡/摩尔,这是20个靶点中总结合分数最低的(表S3)。
使用直方图和箱线图分析结合模式,以探究LF化合物如何与关键靶点相互作用。按总结合分数排序的直方图展示了20个靶点的结合亲和力分布(图2A)。根据对接结果,这些靶点被分为四组(I- IV),其中包含排名前五的靶点的I组被预测与LF化合物结合最紧密,这表明它们在控制尿酸方面发挥着关键作用。大多数LF化合物与I- III组的靶点具有中等结合亲和力(-7至-9千卡/摩尔),而IV组靶点(如GH05、GH13、GH08和GH12)与更多弱结合化合物相互作用(\((>-6 kcal / mol)\))。箱线图进一步详细展示了结合亲和力的分布,为LF化合物与其靶点之间的相互作用提供了见解。
确定的10种高结合亲和力化合物为GQ164、GQ171、GQ165、GQ116、GQ036、GQ038、GQ008、GQ037、GQ057和GQ162(图2B)。有趣的是,在排除药物靶点后,GQ164、GQ171、GQ165、GQ116、GQ036和GQ038仍保持在前十名,这表明它们与多个尿酸相关靶点相互作用,具有多靶点药物开发的潜力。结合稳定性的箱线图显示,四分位距越小,结合亲和力越强;而四分位距越大,则结合力越弱。
在排名前十的化合物中,GQ162的异常值范围最小,其次是GQ165和GQ171,这表明它们与每个靶点的结合都很稳定。GQ164的平均结合能最低(-9.2千卡/摩尔),显示出与所有靶点的稳定相互作用。GQ038和GQ037的平均结合能分别为-8.7千卡/摩尔和-8.6千卡/摩尔,它们与特定靶点(如GH01和GH07)的结合能力较强,但与其他靶点(如GH12-GH20)的结合能力仅为中等水平。在多种蛋白质中具有稳定作用的化合物是开发广谱降尿酸药物的关键。
雷达图显示了排名前十的化合物针对不同靶点的性能(图2C和D)。每种颜色代表一种化合物,越靠近中心的化合物表明其结合能力越强。GH12-GH20显示出较高的结合能,而GH01和GH07更靠近中心,这表明它们是LF化合物降低尿酸所针对的关键蛋白质。在所有靶点中,GH01(XDH)的平均结合能力最高(-7.5千卡/摩尔)。
接下来,我们基于LF中每个靶点的前10种活性化合物以及所有20个靶点构建了一个化合物-靶点网络(图4)。该网络旨在阐明生物活性化合物与其相应蛋白质靶点之间的复杂相互作用,从而为潜在的作用机制提供见解。
通过生物信息学分析深入理解复杂生物系统
该网络(图1C)包含20个节点和59条边,平均节点度为5.9,局部聚类系数为0.668。节点代表靶点,边代表蛋白质间的关联,不同的边颜色表示特定的相互作用。预期的边数为16条,但该网络显示出明显更多的连接,表明其生物连通性高于预期。这些靶点被分为三个聚类:微小RNA介导的基因沉默、有机阴离子转运和5-羟色胺代谢。
KEGG富集分析(图1D)鉴定出9条通路,包括代谢通路,其中精氨酸和脯氨酸代谢通路的P值最低。该通路涉及ALDH2、MAOA和NOS3,这些在高尿酸血症患者和健康人之间存在显著差异(Shen等人,2021年)。其他通路包括与神经相关的通路(血清素能突触)、肿瘤相关通路(VEGF信号通路和抗叶酸通路)、信号转导通路以及脂质代谢通路。在气泡图中,颜色和大小分别代表P值和基因数量,涉及尿酸代谢的代谢通路(PNP、ALDH2、MAOA、NOS3、PTGS2和XDH)包含的靶标比例最高(37.5%)。
对16种与LF相关的蛋白质进行GO富集分析(图1E)发现显著的聚类包括生物过程(BP)、细胞成分(CC)和分子功能(MF)中的三个。最显著的生物过程是无机阴离子转运,而关键的分子功能是有机阴离子跨膜转运蛋白活性。所有细胞成分聚类都与细胞膜相关,这支持了乳铁蛋白(LF)可能通过影响尿酸阴离子的跨膜转运来降低尿酸的假设。鉴于尿酸主要以可溶性尿酸阴离子的形式循环,且先前的研究已发现了转运尿酸的膜蛋白(Chiba等人,2015年;Miyaji等人,2013年),我们推测乳铁蛋白(LF)通过影响尿酸阴离子的跨膜转运发挥了降尿酸作用。
图1. 枸杞治疗高尿酸血症靶点的识别与富集分析。(A) 来自TCMSP、STP和CTD的枸杞(LF)相关靶点与高尿酸血症相关靶点的韦恩图。(B) 13个交叉靶点和7个已知药物靶点。(C) 枸杞靶点的蛋白质-蛋白质相互作用网络。(D) 枸杞靶点的KEGG富集分析,显示排名前9的通路。(E) 枸杞靶点的GO富集分析,包括关键的生物学过程、组成部分和功能。
图2. 188种枸杞化合物与20个高尿酸血症靶点的对接结果。(A) 188种化合物针对20个靶点的结合能直方图。(B) 排名前10的化合物的结合亲和力箱线图。(C) 排名前10的化合物针对各靶点的结合亲和力雷达图。(D) 基于相似性和结合亲和力的枸杞化合物聚类网络。
图3. 枸杞中8个配体与XDH的结合模式。上图显示XDH蛋白(蓝色)及配体结合位点(黄色)。下图详细展示了配体(绿色)与XDH氨基酸通过氢键(绿色线条)或其他相互作用形成的相互作用,键距为\(\AA.\)(关于本图例中颜色的解释,请读者参考本文的网络版本。)
图4. 枸杞治疗高尿酸血症的化合物-靶点网络。该网络显示了排名前10的枸杞化合物(粉色圆圈)与20个靶点(蓝色三角形)之间的相互作用。节点大小和颜色深浅反映度值,节点越大、颜色越深表示度值越高。灰色线条连接靶点与相应的化合物,突出显示相互作用。(关于本图例中颜色的参考解释,读者可查阅本文的网络版本。)
3.4. 枸杞中188种化合物的聚类分析
我们分析了188种LF化合物的结构特性及其与高尿酸血症相关的靶点,重点关注结构与结合亲和力之间的关系。黄嘌呤脱氢酶(XDH)作为降尿酸药物的关键靶点,在分子对接中表现出最高的结合能,因此被用作比较标准。LF化合物与已知的XDH抑制剂非布司他和别嘌醇的结构相似性极低,这可能解释了天然药物与合成药物之间的差异。
在簇网络(图2D)中,化合物按结构相似性分组,结合能随颜色变化而降低变为蓝色。最大的簇包含类固醇、类固醇衍生物和异戊烯醇脂质,对XDH表现出最高的结合亲和力。另一个关键簇含有类固醇和类固醇衍生物化合物,显示出最高的平均结合能,这与之前关于XO抑制的研究(Pereira等人,2018年)一致。因此,我们研究中鉴定出的类固醇和类固醇衍生物可能在LF化合物与XDH的生物相互作用中发挥重要作用,具有作为XDH抑制剂的潜力。与非布司他和别嘌醇的比较显示没有强烈的关联性,但GQ164与非布司他最相似,GQ039与别嘌醇最相似,这表明它们有潜力成为新型候选药物(图S2)。
3.5. 基于黄嘌呤脱氢酶活性位点的枸杞化合物ADMET筛选
根据文献记载,在电子显微镜下观察到非布司他与黄嘌呤脱氢酶(XDH)的四个活性位点结合(Okamoto等人,2003年)。分子对接结果显示,来自LF的121种化合物在这些活性位点附近与XDH发生相互作用。此外,通过ProteinPlus平台,我们确定了XDH的多个结合口袋,并筛选出14种结合于P_0口袋的化合物,共计135种化合物用于进一步分析(表S6)。
使用ADMET Lab 2.0对非布司他活性结合位点中的121种化合物以及P_0口袋中的14种化合物的SMILE序列进行了分析。纳入标准为:(1)0个PAINS警报;(2)0次违反Lipinski五规则;(3)\(H-HT ≤0.7\);(4)肠道\(absorption ≥30 \%;\);(5)无Ames毒性;(6)无致癌性;(7)结合\(energy <-6 kcal / mol\)。结果显示,有8种化合物符合这些标准,它们与XDH有较强的相互作用,且具有类药物特性和无毒性潜力。这些化合物分别是GQ046(1,1,6-三甲基-2H-萘)、GQ049(β-谷甾醇)、GQ066(菜油甾醇)、GQ067(牡蛎甾醇)、GQ086(黄豆黄素)、GQ118(24-乙基胆甾-5,22-二烯醇)、GQ122(岩藻甾醇)和GQ181(钝叶甾醇)(表S4和S5)。
3.6. 分子动力学模拟预测黄豆苷元是与黄嘌呤脱氢酶结合最稳定的配体
接下来,我们详细分析了这八种化合物的分子对接构象(图3)。氢键对于分子间相互作用、复合物的形成和稳定性至关重要(Tripathi和Bandyopadhyay,2022;Willett,1995)。在这八种化合物中,只有GQ046、GQ067和GQ181没有与XDH形成氢键。GQ049与XDH的Asp59和Lys57结合,氢键距离分别为\(2.21 A\)和\(1.84 元\)。GQ066在Asp360残基的\(1.91 A\)处结合。GQ086在Ser347残基的\(2.84 A\)处结合。GQ118分别与Asp430和Lys422残基的\(3.06 \AA\)和\(2.83 \AA\)结合。GQ122在\(2.93 \AA\)处与Gly350残基结合。这些相互作用凸显了氢键在配体-蛋白质结合中的重要性,以及这些化合物作为治疗剂的潜力。虽然三种化合物在计算机模拟中未显示出氢键,但为了考虑潜在的体内相互作用,它们仍被纳入分子动力学模拟研究中。
在对8个小分子与XDH蛋白的结合动力学进行50纳秒的模拟后,我们利用均方根偏差(RMSD)、均方根波动(RMSF)、回转半径\((R_{g})\)、溶剂可及表面积(SASA)以及氢键数量等参数,对其稳定性和相互作用强度进行了严格评估。尽管GQ046展现出良好的特性,但由于在模拟中未形成氢键而被排除。其余7种化合物的模拟结果如图5所示。
在模拟的初始阶段,系统会经历较大的能量和结构波动,直至达到稳定状态。如图5A所示,配体-蛋白质复合物在系统弛豫约10纳秒后达到平衡。随后,我们总结了7种配体-蛋白质复合物在10-50纳秒内的平均轨迹结果,如表1所示。
RMSD 测量原子的平均位置偏差,反映分子随时间的稳定性。图 5A 显示所有系统均在50纳秒内相对稳定,没有超过0.25纳米的重大位移。脱辅基蛋白的平均RMSD为0.243纳米,紧随其后的是结合GQ066的蛋白,为0.237纳米。除了XDH-GQ049和XDH-GQ118之外,所有其他复合物的平均RMSD值都低于脱辅基蛋白,这表明配体结合提高了稳定性。在所有配体-蛋白复合物中,GQ067最稳定,平均RMSD为0.206纳米,紧随其后的是GQ122和GQ086,平均RMSD值分别为0.107纳米和0.213纳米。在所有七种配体中,GQ086的平均RMSD值最低,为0.04纳米(图5B),表明其在XDH活性位点的结合更稳定。
\(R_{g}\)和SASA的变化可以揭示模拟过程中蛋白质的结构变化及其对环境变化的响应。\(R_{g}\)用于测量分子的致密性,其值越小表明致密性越高。所有系统的标准差均在0.01纳米以下,且无显著变化(图5C),这表明蛋白质构象稳定且致密。GQ067结合蛋白和GQ118结合蛋白的\(R_{g}\)平均数值最高,为3.221纳米,两者在20-30纳秒期间均表现出更多的解折叠现象。这两种复合物的SASA值也最高(图5D),并且是仅有的两种SASA值高于脱辅基蛋白的复合物,这表明与这些配体结合会导致蛋白质展开或不稳定。相比之下,其他五种配体降低了SASA值,表明黄嘌呤脱氢酶(XDH)结构更致密,这支持了\(R_{g}\)的研究结果。
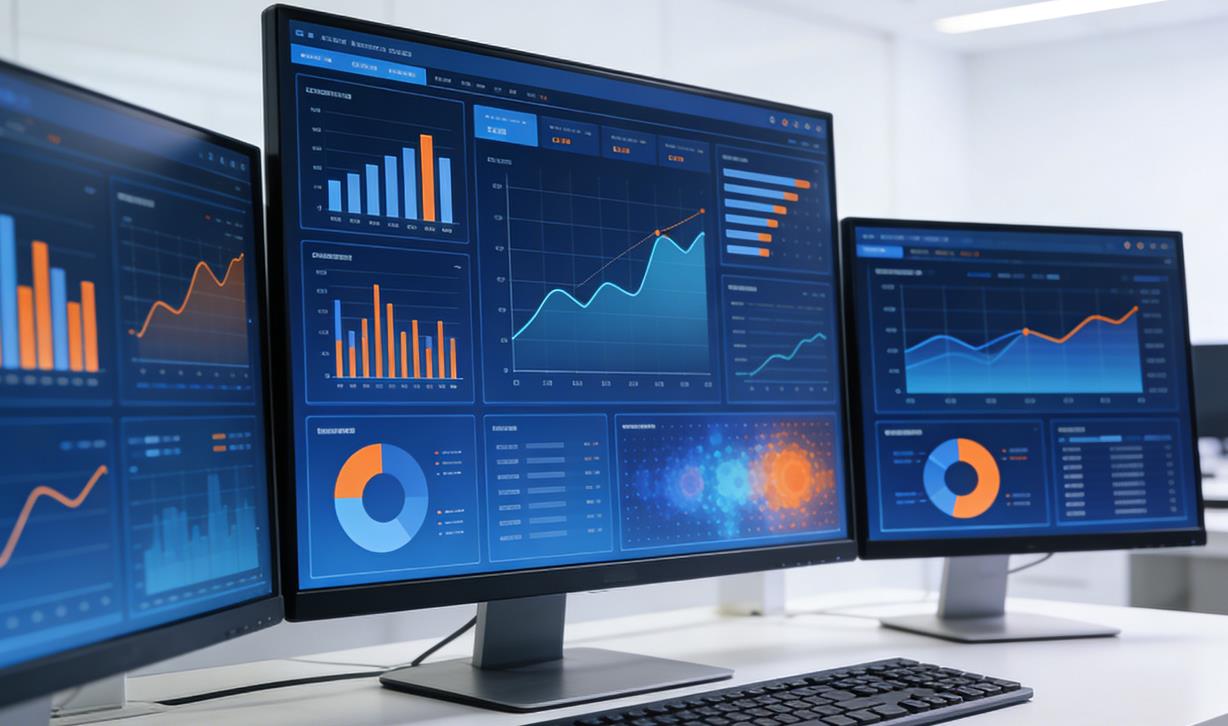
如图5E和F所示,RMSF的变化主要集中在Thr750到Val1333之间的结合位点残基上。峰值在环区域大量重叠,谷值也呈现类似趋势,尤其是配体结合结构。在Glu1144、His1286和Glu1324附近观察到了RMSF的细微差异(图5E中突出显示)。Glu1144和Glu1324附近的复合物表现出比蛋白质本身更高的RMSF值,这意味着这些区域具有更高的灵活性或动态性,而His1286和Thr1315附近的残基波动受到抑制,表明它们对配体结合和蛋白质稳定性具有重要意义。所有复合物的其他RMSF变化均相似,突变研究可以进一步阐明这些区域的生物学意义。
0.35 nm范围内的氢键数量和氢对数量分别如图5G和图5H所示。在整个50 ns的模拟过程中,GQ086保持了最多的氢键数量,其次是GQ118和GQ046,这与配体的均方根偏差结果(图5B)一致。GQ066、GQ067、GQ122和GQ181通常只有不到一个氢键对,这是由于配体构象变化导致的断裂。总体而言,GQ086在与XDH的结合中表现出最佳的稳定性。
3.7. 体外和体内验证,以确认大豆苷元可通过靶向黄嘌呤脱氢酶来降低尿酸
为了证实黄豆苷元靶向黄嘌呤脱氢酶(XDH)的效果,我们开展了一系列研究。首先,有必要证明黄豆苷元存在于LF中。为验证这一点,我们采用非靶向代谢组学分析LF中的成分。图6A显示了通过LC-MS/MS(UPLC-Q-Exactive Plus)在正负离子检测模式下测得的LF样品质谱基峰图。在负离子模式下,检测到206种已知化合物,而在正离子模式下鉴定出326种已知化合物。通过使用质荷比283.06、离子保留时间9.55分钟和分子式\(C_{16} H_{12} O_{5}\)检索四个数据库,证实了LF中存在黄豆苷元(表S8)。
接下来,我们评估了黄豆苷元是否能有效降低尿酸水平。参考先前的研究(Wei等人,2022年;Zhang等人,2019年),我们建立了高尿酸血症斑马鱼模型(图6B),并给予三种不同浓度的黄豆苷元,分别为25、50和100μM(1/4、1/2和最大耐受浓度)(图S5)。与对照组相比,模型组的尿酸水平显著升高\((p<0.05)\),这证实了高尿酸血症斑马鱼模型的成功建立。值得注意的是,浓度为100μM的黄豆苷元显著降低了高尿酸血症斑马鱼的尿酸水平(\((p<0.05)\)(图6C)。
图5. 基于分子动力学模拟对空载、GQ049、GQ066、GQ067、GQ086、GQ118、GQ122和GQ181结合的XDH的结构分析。七种抑制剂的部分参数值如下所示,包括蛋白质RMSD(A)、配体RMSD(B)、\(R_{g}\)(C)、SASA(D)、RMSF(E)、RMSF变化(F)、氢键数量(G)以及0.35毫米内的配对数量(H)。
不同组别的XOD酶活性抑制率如图6D所示。DMSO对照组的抑制率为8.01±2.16%。经ALP处理的阳性对照组表现出显著更高的抑制率,为80.54+2.51% \((p<0.001)\)。在大豆苷元处理组中,抑制率随浓度变化,其\(IC _{50}\)值为1.39 M。100 M大豆苷元组的抑制率最高,为92.39+3.68% \((p<\) \(0.001\)),超过了阳性对照组。10 pM和1 pM大豆苷元组的抑制率分别为71.32±6.18%和73.65±6.92% \((p<0.001)\)。最低浓度(0.1 M大豆苷元)的抑制率为66.55+2.07% \((p<0.05)\),虽低于较高浓度组,但仍显著高于DMSO对照组。
我们还进行了细胞热迁移分析,以研究黄豆苷元是否能增强XDH蛋白的稳定性。在50°C至70°C的温度梯度下监测蛋白质表达,发现二甲基亚砜对照组和黄豆苷元处理组之间存在显著差异。如图6E和F所示,黄豆苷元处理组在高温下表现出更高的稳定性,尤其是在65°C和70°C时\((p<0.05)\)。这一发现表明,黄豆苷元可能与AML12细胞中的XDH蛋白直接相互作用并使其稳定。总之,体外和体内实验均证实了黄豆苷元的降尿酸作用及其与XDH蛋白的相互作用。
3.8. 利用分子对接阐明的额外黄豆苷元结合位点及与黄嘌呤脱氢酶的相互作用
实验研究证实,黄豆苷元具有降低尿酸水平的能力,这促使研究人员使用Autodock 4.2并结合Mo(VI)参数进行进一步的对接计算,以确定黄豆苷元在黄嘌呤脱氢酶(XDH)上的其他潜在结合位点,并探究钼辅因子可能产生的影响。
在300次黄豆苷元与1N5X(分类:牛;一致性百分比:89.56%)的对接实验中(包含钼蝶呤),与之前描述的2CKJ(分类:智人;一致性百分比:100%)相比,只有6个模型中黄豆苷元位于非布司他结合位点附近(图S7,左侧位点)。其中,在300次对接实验的2个黄豆苷元模型中,黄豆苷元与Arg880形成了氢键,但未观察到与其他三个关键残基(Thr1010、Asn768和Glu802)的相互作用。此外,所有预测模型均未与钼辅因子紧密接触。
值得注意的是,非布司他通过与Arg880相互作用疏水相互作用,并与主要关键残基Thr1010、Asn768和Glu802形成氢键,这些残基对稳定性至关重要。另一方面,Arg880似乎能稳定结构,以支持与这三个关键残基形成氢键。总体而言,大豆黄素缺乏与主要关键残基的相互作用,仅与黄嘌呤脱氢酶形成一个氢键,而非布司他则形成三个氢键。这导致大豆黄素在这些位置的结合亲和力较弱(范围为-5.9千卡/摩尔至-6.62千卡/摩尔),显示出它们的结合机制存在明显差异。此外,盲对接还揭示了在P_0位点可能存在的结合位置(图S7,右侧位点),这与上文详述的使用ProteinPlus服务器确定的有利口袋位置一致。
3.9. 延长200纳秒分子动力学模拟以阐明黄豆苷元与黄嘌呤脱氢酶的长期相互作用
上述研究证实了黄豆黄素的降尿酸作用及其与黄嘌呤脱氢酶(XDH)的结合亲和力。为评估其长期潜力,我们将分子动力学(MD)模拟延长至200纳秒,并进行了三次重复实验,以更全面地了解黄豆黄素与XDH的长期相互作用。为便于比较,在相同条件下对别嘌醇结合的XDH也进行了模拟。图7比较了空载XDH和黄豆黄素结合的XDH随时间的变化。在10纳秒达到平衡后,黄豆黄素保持了稳定的均方根偏差(RMSD)、\(R_{g}\)和溶剂可及表面积(SASA)值(分别为0.239纳米、3.213纳米和\(490.061 \AA^{2}\)),与空载XDH(0.255纳米、3.221纳米和\(493.218 \AA^{2}\))和别嘌醇结合的XDH(0.250纳米、3.218纳米和\(493.119 \AA^{2}\))相当。如图7(A-C)所示的RMSD、\(R_{g}\)和SASA值所反映的,黄豆黄素的结合提高了蛋白质折叠的紧凑性和稳定性。
模拟还显示氢键数量在增加,最初为1到2个,7纳秒后增至2.5个,并在75纳秒后趋于稳定(图7D)。尽管0.35纳米范围内的配对数量(图7F)在20纳秒系统弛豫后不久略有下降,但波动保持一致,呈现出近似周期性的模式。黄豆苷元的均方根偏差(RMSD)保持较低水平(0.048纳米),表明其与黄嘌呤脱氢酶(XDH)的结合稳定(图7H)。快照显示,在整个200纳秒的模拟过程中,黄豆苷元(蓝色范德华表面)始终紧密结合在XDH(橙色卡通模型)的活性口袋中(视频S1)。图7G中的残基均方根波动(RMSF)图进一步支持了时间序列分析,表明在黄豆苷元结合后,XDH活性位点残基的稳定性更高,波动更小。具体而言,谷氨酰胺1041(Gln1041)和赖氨酸1173(Lys1173)在配体结合后变得更加刚性,RMSF值更低。三个例外是天冬酰胺1146(Asn1146)、精氨酸1246(Arg1246)和缬氨酸1291(Val1291),这些残基位于远离黄豆苷元结合位点的位置。总体而言,200纳秒的分子动力学模拟表明,黄豆苷元能稳定结合XDH,这支持了其作为XDH抑制剂的潜力,并为为未来药物开发提供有价值的基础数据。
图6. 黄豆苷元对高尿酸血症和黄嘌呤脱氢酶(XDH)抑制作用的验证。(A)枸杞的非靶向代谢组学分析。x轴代表保留时间(分钟),范围为0至20分钟,y轴表示信号强度。每个峰对应枸杞中检测到的一种独特化合物。(B)高尿酸血症斑马鱼模型的建立(\(n=3\) \(^{*} p<0.05\)与DMSO对照组对比)。(C)黄豆苷元处理(100、50、25μM)对高尿酸血症斑马鱼模型的尿酸降低作用(\(n=3\) \(^{*+*} p<0.001\)与DMSO对比,\(\phi \phi \phi p<0.001\)与模型组对比,\(^{*} p<0.01\)与模型组对比)。ALP(别嘌醇,100pM)作为阳性对照。(D)0.1、1、10、100M黄豆苷元对黄嘌呤氧化酶(XOD)活性的抑制作用(\(n=4\),\(p<0.01\) 3 \(^{*} p<0.05\)/s. ALP)。(E)DMSO处理组(上)和黄豆苷元处理组(下)在不同温度(50℃、55℃、60℃、65℃、70℃)下XDH蛋白的细胞热位移分析。(F)(E)的定量分析(\((n=4\) \(^{\circ} p<0.05\))。
图7. 基于三次200纳秒分子动力学模拟的平均结果对结合黄豆黄素的XDH进行结构分析。所分析的参数包括(E)蛋白质均方根偏差(RMSD)、(F)回转半径\((R_{g})\)、(G)溶剂可及表面积(SASA)、(H)配体均方根偏差(RMSD)、(I)氢键数量、(J)0.35纳米内的配对数量、(K)均方根波动(RMSF),以及(L)XDH残基随时间(1纳秒、50纳秒、100纳秒、150纳秒、200纳秒)的结构表征。空载蛋白值以橙色显示,结合黄豆黄素的蛋白值以蓝色显示。(关于本图图例中颜色的解释,读者可参考本文的网络版本。)
讨论
近年来,科学家们一直致力于从天然活性成分中筛选黄嘌呤氧化酶(XOD)抑制剂。这些天然化合物相较于合成药物具有诸多优势,例如成本更低、副作用更少,这使它们成为预防高尿酸血症的潜在物质。类黄酮作为一类存在于水果、蔬菜、茶叶等天然产物中的天然抑制剂,具有多种生物活性且毒性较低,近年来引起了广泛关注。保罗·科斯发现,类黄酮中C-5和C-7位的羟基以及C-2和C-3位之间的双键可能有助于降低黄嘌呤氧化酶的活性(Wan等人,2021年)。
我们在LF中发现的黄酮类化合物黄豆黄素,具有一个与苯环稠合的苯并吡喃酮核心,已知其具有抗氧化、抗炎和酶调节特性(Al-Khayri等人,2022年)。在本研究中,我们从LF中鉴定出黄豆黄素是一种生物活性化合物,并证实了其降尿酸作用。LF是一种常见的食用食品,在传统医学中长期被用于治疗高尿酸血症。虽然先前的研究表明LF提取物具有降低尿酸的能力,但我们的研究结果为黄豆黄素在这一过程中的作用提供了确凿证据。
通过全面的生物信息学分析,我们确定了20个潜在靶点(图1A和B),它们的蛋白质-蛋白质相互作用网络(图1C)显示出很强的相关性。京都基因与基因组百科全书(KEGG)通路富集分析(图1D)表明,最富集的通路是代谢通路,涉及6个基因(PNP、ALDH2、MAOA、NOS3、PTGS2和XDH),这凸显了乳铁蛋白(LF)与尿酸代谢之间多方面的生化相互作用。乳铁蛋白可能通过多种代谢途径降低尿酸盐。p值最小的通路是精氨酸和脯氨酸代谢(涉及ALDH2、MAOA和NOS3),这表明乳铁蛋白在调节一氧化氮合成和尿素循环方面具有潜在作用,而这两者对尿酸代谢都很重要。NOS3的参与表明其对肾功能和尿酸排泄有影响。这些发现支持乳铁蛋白作为一种多靶点方法来管理高尿酸血症,并为未来的药物开发提供了见解。基因本体论(GO)富集分析(图1E)强调无机阴离子转运是一个关键的生物学过程,表明乳铁蛋白可增强尿酸排泄。有机阴离子转运体活性进一步支持了乳铁蛋白在尿酸清除中的作用,而顶端质膜的参与则会影响尿酸的重吸收和分泌。
在分子对接中,超过50%的LF化合物对20种靶蛋白表现出高结合亲和力(低于-6.0千卡/摩尔)(表S3和S4),其中27种化合物的结合能低于非布司他(-8.7千卡/摩尔)。平均结合能最低的前10种化合物对超过一半的靶蛋白表现出强结合亲和力(图2B和C),因此被视为多效化合物。对结合蛋白靶标的分析(图2A)以及每个靶标类别的结合能直方图表明,相当数量的配体对组(I)中的靶标表现出良好的结合亲和力。值得注意的是,被鉴定为XDH的GH01显示出最佳的平均结合结果,与大多数配体对接时具有优异的结合分数(低于-9.0千卡/摩尔)。基于每个靶标和所有20个靶标对应的LF叶中前10种活性化合物,我们构建了一个化合物-靶标网络(图4)。通过绘制这些相互作用网络,我们确定了可能有助于LF治疗效果的关键化合物。此外,这种全面的网络分析有助于发现新的生物活性化合物,并促进靶向抑制剂的开发。
分子对接结果表明,XDH是进一步研究的关键靶点。XDH基因编码黄嘌呤氧化还原酶蛋白,该蛋白包括XDH和XO(Dissanayake等人,2024)。XDH在嘌呤代谢中至关重要,可将次黄嘌呤转化为黄嘌呤,进而转化为尿酸(Siu等人,2006)。XDH还可以转化为XO,进一步促进尿酸的生成(Chen、Guo等人,2023)。鉴于其双重作用,我们将重点放在化合物上。能够结合并可能抑制XDH。
聚类分析显示,一些LF化合物因结构相似性形成了簇,主要为类固醇及类固醇衍生物、异戊烯醇脂质、饱和烃和脂肪酰基(图2D)。最大的簇具有与XDH良好的结合亲和力,主要包含类固醇及类固醇衍生物和异戊烯醇脂质。另一个值得注意的簇包含8种化合物,均为类固醇及类固醇衍生物,在所有簇中表现出最高的平均结合能。这些化合物可能通过调节炎症反应影响尿酸水平,从而减少尿酸生成(Barton & Frigo,2021)。先前的研究表明,具有特定结构的化合物具有显著的XO抑制作用(Pereira等人,2018)。因此,本研究中发现的类固醇及其衍生物可能在LF化合物与XDH的生物相互作用中发挥关键作用,有望成为潜在的XDH抑制剂。这些化合物可能是开发新型XDH抑制剂的宝贵候选物。
为了从枸杞中筛选出有潜力的候选配体,我们最初的目标是找到能与非布司他结合的相同四个关键氨基酸残基(Arg880、Thr1010、Asn768、Glu802)结合的化合物。然而,没有任何化合物能直接与这些残基相互作用。需要注意的是,不能与这些特定残基相互作用并不意味着它们与抑制机制无关。相反,我们的方法基于更广泛的策略。我们筛选出了119种位于这些残基附近的化合物,这表明它们可能与非布司他结合在同一个可成药口袋中。
此外,借助ProteinPlus平台,我们预测了替代结合口袋,并选择了得分最高的口袋P_0。该口袋内的化合物也被纳入了我们的分析中。为了筛选出假阳性结果,我们进行了PAINS测试,随后利用ADMET标准对化合物进行评估。最终,确定了8种符合对接、PAINS和ADMET标准的配体(表S5)。这些化合物的平均结合能介于-8.1至-6.9千卡/摩尔之间,且所有分子在PAINS测试中均未出现警示。除GQ046和GQ181外,其余7种化合物均形成了一个或多个氢键(图3)(表S5)。
接下来,我们进行了50纳秒的分子动力学模拟。这一模拟时长是根据以往的研究(Hasan等人,2024年;Xiong等人,2022年)确定的,其中包括针对多化合物模拟的更短的20纳秒方案(Yakoubi,2024年)。我们旨在快速筛选这8种化合物作为高尿酸血症中的黄嘌呤脱氢酶抑制剂,并重点研究系统稳定后10-40纳秒内的复合物行为。由于在整个50纳秒的模拟过程中均未形成氢键,GQ046被排除在外。配体结合复合物(图5)在构象稳定性、蛋白质紧凑性和波动行为方面与无配体蛋白质呈现出相似的趋势。值得注意的是,与脱辅基蛋白质(0.243±0.029纳米)相比,别嘌醇结合系统(图S7A)和GQ086结合系统均表现出更低的蛋白质均方根偏差值(分别为0.212±0.019纳米和0.213±0.013纳米),这表明配体结合后稳定性有所增强。随时间变化的均方根偏差分析(图5A和B)显示,配体存在时位移更大,但所有7个配体-蛋白质系统都达到了平衡。
LF化合物诱导的蛋白质RMSD值(0.206–0.291 nm)与槲皮素(0.25 nm)、木犀草素(0.27 nm)等天然化合物(Pathak等人,2018年)以及临床使用的黄嘌呤脱氢酶(XDH)抑制剂别嘌醇(较长模拟中为0.43 nm,Pan等人,2021年)的RMSD值相当或更低。在我们50纳秒的模拟中,别嘌醇的RMSD较低(0.212 nm),这表明较短的时间尺度可能低估了结构重排,而GQ086在相同时间范围内达到了相当的稳定性(0.213 nm)。尽管RMSD值相对稳定,但平均\(R_{g}\)和溶剂可及表面积(SASA)测量值(图5C和D)与另一项研究(Pan等人,2021年)相差约0.32 nm和\(169 ~nm^{2}\),这表明蛋白质结构存在细微差异,因为这种酶以两种可相互转化的形式存在:黄嘌呤脱氢酶(XDH)和黄嘌呤氧化酶(XO)。在我们的模拟中,结合别嘌醇(图S7A–C)和结合GQ086的黄嘌呤脱氢酶(XDH)显示出相似的\(R_{g}\)(3.221±0.006 nm对3.217±0.005 nm)和溶剂可及表面积(SASA)值(\(498.398 \pm 4.330 \AA^{2}\)对\(493.986 \pm 5.655 \AA^{2}\)),这表明相当的构象紧凑性。
RMSF值(图5E和F)与类似的酶分子动力学模拟研究中的值相当。在我们的研究中,与别嘌醇相比,结合GQ086的XDH在关键残基(如Gln803、Gln958和Glu1144)中表现出更低的波动(图S7D),这意味着尽管整体RMSF相近(0.120±0.08 nm对0.116±0.774 nm),但局部稳定性更强。这与黄嘌呤氧化酶(XO)的研究(Pan等人,2021年)形成对比,在该研究中,配体结合通常会增加活性位点的灵活性。
氢键分析(图5G)显示,GQ086与黄嘌呤脱氢酶(XDH)残基形成的极性相互作用最多。尽管这些极性相互作用在50纳秒的时间尺度内存在波动,但与GQ066等其他配体相比,其一致的模式表明在结合口袋处存在稳定且强烈的相互作用。还需要进一步开展突变研究,重点关注通过对接和模拟确定的与配体相互作用的残基,以明确这些极性相互作用在XDH抑制中的作用。总之,GQ086具有较高的结合稳定性、紧凑性以及极性相互作用,这表明其有潜力成为未来XDH抑制剂的候选物,后续实验进一步支持了这一结论。
体外实验证实,大豆黄素可抑制XOD活性(图6D)。大豆黄素的\(IC _{50}\)为1.39M,而阳性对照药别嘌醇和另一种天然XOD抑制剂槲皮素的\(IC _{50}\)分别为0.24μM和2.6μM(Cos等人,1998年)。大豆黄素的XOD抑制效果约为别嘌醇的1/6,且达到50%抑制所需的大豆黄素浓度比槲皮素低约2倍。这些结果表明,如果大豆黄素被人体吸收,与槲皮素相比,它可能作为一种更有效的XO活性抑制剂发挥作用。
我们的实验证据表明黄豆苷元能够降低尿酸水平,这促使我们开展了额外的盲对接研究,重点关注该配体与黄嘌呤脱氢酶(XDH)的相互作用,包括与钼辅因子的作用。大量的对接计算预测,黄豆苷元不会与钼辅因子紧密结合,但会与精氨酸880(Arg880)形成氢键,而该位点靠近三个已知能结合非布司他的关键残基(苏氨酸1010、天冬酰胺768和谷氨酸802),这些残基对非布司他的结合稳定性至关重要。这些发现表明,黄豆苷元的抑制机制与非布司他不同。尽管黄豆苷元不会与主要残基结合,但我们发现了一个替代结合位点,目前将其称为XDH的P_0口袋。该区域可能在黄豆苷元对XDH的抑制作用中发挥作用,这或许能解释其降尿酸特性。总之,这些对接结果显示,作为天然化合物的黄豆苷元和作为合成抑制剂的非布司他与XDH的相互作用方式不同,尽管黄豆苷元可能不会直接与钼辅因子紧密结合,也不会与非布司他结合相同的残基,但其降尿酸作用可能与它与替代结合位点(如P_0口袋)的相互作用有关。
XOD和XDH是结构和功能上同源的酶,均来源于同一基因。鉴于它们的相似性,观察到的XOD抑制现象表明,大豆黄素可能也会对XDH产生潜在的抑制作用。为进一步验证这一假设,我们进行了细胞热迁移分析(图6E和F),结果显示大豆黄素显著提高了AML12细胞中XDH的稳定性——选择该细胞系是因为其肝XDH表达量高(Huang等人,2023年)。
虽然我们已经证实了黄豆苷元在体外对黄嘌呤脱氢酶(XDH)的作用,但类黄酮在体外和体内的酶活性强度会受到其化合物结构和生物利用度的影响。许多化合物在体外显示出较强的作用,但这些作用并不总能转化为较高的体内疗效。因此,我们进行了进一步的体内研究,以验证黄豆苷元潜在的治疗应用。高尿酸血症斑马鱼模型证实了黄豆苷元的降尿酸作用,高剂量黄豆苷元的疗效与别嘌醇相当(图6C)。由于斑马鱼与人类在基因上具有相似性,它们为研究黄豆苷元对尿酸代谢的影响提供了宝贵的见解。观察到的尿酸水平降低支持了黄豆苷元作为一种(潜在药物的可能性)。治疗高尿酸血症的药物。这些结果,连同斑马鱼模型的实时观察能力和高通量筛选能力,为在更高阶模型(如小鼠模型)中进一步研究黄豆苷元的临床潜力奠定了基础。
分子动力学模拟延长至200纳秒,为黄豆黄素-XDH复合物的长期稳定性和行为提供了见解(图7)。为确保结果的可靠性,我们对黄豆黄素和别嘌醇(阳性对照;图S7E-H)均进行了三次重复模拟,并对平均值进行了分析。结果表明,黄豆黄素的均方根偏差(RMSD)、\(R_{g}\)以及溶剂可及表面积(SASA)与脱辅基XDH蛋白处于相近水平,这表明蛋白结构结合稳定且紧凑性增强。值得注意的是,黄豆黄素表现出与别嘌醇相当的整体稳定性,且关键功能区域的残基波动(RMSF)略有降低,这进一步支持了其作为竞争性XDH抑制剂的潜力。模拟过程中观察到的氢键频率增加,进一步证实了黄豆黄素与XDH之间存在稳定的相互作用。
尽管我们的研究成功在体内利用斑马鱼证明了黄豆黄素的降尿酸作用,但并未在该模型中充分验证黄豆黄素与黄嘌呤脱氢酶(XDH)之间的相互作用。黄嘌呤脱氢酶有三个催化区域(Kumar等人,2018年),其中一个包含钼辅因子。钼辅因子区域在该酶的催化活性中起着重要作用,因为它参与次黄嘌呤氧化为尿酸过程中的电子传递。虽然钼辅因子在黄嘌呤氧化酶(XOD)抑制中作用显著,但我们的结果并未显示其与钼辅因子区域存在直接相互作用。基于分子动力学模拟,黄豆黄素对接在黄嘌呤脱氢酶的非催化区域,与位于钼辅因子区域之外的SER347形成氢键。因此,黄豆黄素的抑制作用并不涉及与钼辅因子的直接结合。然而,黄豆黄素是否间接影响钼区域或对其他催化结构域(如Fe-S或NAD)产生作用,仍有待通过体内研究进一步探究。这一观察结果与近期的研究(Guo等人,2023年)一致,即一些新型黄嘌呤氧化酶抑制剂通过与钼辅因子以外的位点相互作用来抑制酶活性。
除XDH外,我们之前的研究表明,LF还可能通过调节NOS3促进尿酸排泄,为其降尿酸作用提供了更广泛的机制。此外,LF中含有的高浓度类固醇及其衍生物,以及催化前脂质,表现出最高的平均结合亲和力,这凸显了LF的多靶点潜力。这表明,LF中多种化合物通过靶向不同通路产生的协同效应,仍是未来研究中一个令人期待的领域。
此外,体内结合机制仍有待充分探索,还需要进一步研究来评估黄豆苷元在体内的生物利用度和 efficacy。此外,我们认识到钼辅因子在黄嘌呤氧化酶(XOD)抑制中的作用仍然重要,未来的研究将探究黄豆苷元与钼辅因子结构域之间的相互作用,特别是在啮齿类动物模型中。这将有助于阐明黄豆苷元作用的更广泛机制。未来的研究将重点探索这种在啮齿类动物模型中的相互作用,研究剂量反应和药代动力学,评估长期毒性,并开展初步临床试验,以评估黄豆苷元作为高尿酸血症潜在治疗药物的安全性和有效性。
结论
我们预测了LF在降尿酸方面的通路和生物学功能,发现有13个靶点与其密切相关。其中,通过非靶向代谢组学证实, glycitein是来自LF的一种化合物,它与排名最高的靶蛋白XDH的预测结合亲和力最高。进一步研究表明,glycitein在体外可与XDH结合,且高浓度的glycitein能降低高尿酸血症斑马鱼的尿酸水平,这为高尿酸血症的防治提供了新思路。其生物学活性黄豆苷元在降尿酸方面的作用,也为开发以黄豆苷元为基础的枸杞功能性产品带来了新的机遇,例如枸杞奶茶或枸杞调和油。
关于木芮生物
ABOUT MURUIBIO
苏州木芮生物科技有限公司(以下简称“木芮生物”)成立于2018年1月22日,是一家致力于以斑马鱼为模式生物提供生物医学基础科研服务、斑马鱼实验操作试剂盒、斑马鱼临床疾病模型、其他生物学实验试剂以及进行斑马鱼应用技术转化的高科技公司。
木芮生物以斑马鱼为模式生物,建立起了上百种的临床疾病模型,深入探索相关疾病发生的深层次疾病机制, 进而为临床治疗疾病提供可行的治疗方案或者药物筛选机制。到目前为止,木芮生物已经建立起包括遗传、行为、 细胞、 生化分子等斑马鱼相关成熟的技术,并且依托这些技术成功将斑马鱼应用到基础科研、毒理测试、癌症药物筛选、 中药药效成分筛选、保健品开发和功效评价。
木芮生物经过七年的快速发展,公司现已有核心创业团队成员20余人,其中博士研究生1人,硕士研究生6人,本科生10余人。木芮生物成立后,陆续与江苏省产业研究院和苏州纳米应用技术研究所等科研单位建立起了科研合作,建立了“模式生物技术与应用研发中心”;公司于2020年被认定为“国家高新技术企业”,于 2021年底获得苏州工业园区“领军成长企业”称号。
敬请关注